写在前面
今天推来自西方大学医学生物物理学系成像研究实验室和劳森健康研究所在2018年发表于Cell Discovery(2018IF:4.321,JCRQ2)的一篇文章,通讯作者是John J. Kelly和 John A. Ronald教授。
文章摘要
表达成像报告基因的细胞的无创分子遗传成像是一种在临床前模型和患者中纵向监测癌细胞的生物分布和活力以及基于细胞的疗法的宝贵方法。 然而,用报告基因标记细胞通常依赖于使用将报告基因随机整合到基因组中的基因转移方法,这可能会导致不必要的甚至严重的不利影响。为了克服这个问题,我们开发了 CRISPR-Cas9 工具来编辑腺相关病毒位点 1 (AAVS1) 安全港的细胞,其中包含编码抗生素抗性基因和报告基因的大型供体构建体 (*6.3 kb) 用于生物发光 (BLI)和荧光成像。 HEK293T 细胞在一个质粒中用编码 Cas9 核酸内切酶和 AAVS1 靶向引导 RNA 的双质粒系统转染,以及编码嘌呤霉素抗性基因、tdTomato 和萤火虫荧光素酶的供体质粒,两侧是 AAVS1 同源臂。分离嘌呤霉素抗性克隆细胞,并通过 PCR 和 PCR 产物测序确认 AAVS1 整合。体外 BLI 信号与细胞数密切相关 (R2 = 0.9988; p < 0.05) 并且在多个传代中保持稳定。将工程细胞 (2.5·106) 注射到裸鼠的左后腹,并在第 0、7、14、21 和 28 天进行体内 BLI。BLI 信号从第 0 天到第 7 天呈下降趋势,但到第 28 天,由于细胞生长显著增加 (p < 0.05)。这描述了第一个用于 AAVS1 整合大基因构建体的 CRISPR-Cas9 系统,用于体内细胞的分子遗传成像。随着进一步的发展,包括提高编辑效率、使用临床相关报告基因,以及对其他可以在培养中容易扩增的细胞群(例如永生化细胞或 T 细胞)进行评估,这种 CRISPR-Cas9 报告基因系统可以广泛应用于多项体内细胞追踪研究。
研究背景
基于报告基因 (RG) 的细胞成像,也称为分子遗传成像,可以提供有关移植细胞在活体中的运输、生物分布、活力和持久性的重要信息。可用的 RG 范围涵盖临床前成像模式从荧光成像和生物发光成像 (BLI) 到磁共振成像、光声断层扫描和正电子发射断层扫描 (PET) 等临床模式。在疾病的临床前模型中,基于 RG 的细胞跟踪已经对疾病特征产生了重要的前瞻性,例如癌症转移和新疗法对转移性病变的治疗效果,以及治疗细胞向特定疾病位点的活力和迁移。细胞毒性 T 细胞在高级别胶质瘤患者中的活力。
RG 细胞成像涉及将 RG 整合到细胞的基因组中,以便在细胞的整个生命周期或任何潜在子细胞的生命周期内稳定地产生报告蛋白。这些报告产物的检测提供了有关细胞位置/数量和细胞活力随时间推移的重要间接信息。此外,基于如何调节 RG 表达,例如使用哪个启动子。人们可以获得有关细胞活化和/或分化的信息。虽然这是非常宝贵的信息,但也存在一个问题,工程过程中,与幼稚的细胞相比,细胞的行为可能会发生改变。例如,慢病毒载体是一种流行的工程细胞载体,因为它们具有大的转基因能力,并且能够容易地转导多种分裂和非分裂细胞类型。然而,与大多数整合载体一样,慢病毒载体在准引入基因随机基因组位点有可能导致不想要的事件,例如癌基因激活差异剪接、通读转录和异常转录。因此,在特定基因组区域设计具有 RG 的细胞的新颖、相对易于使用的工具将避免这些问题并具有很大的价值。
基因组编辑工具已经存在了几十年,它允许将感兴趣的转基因整合到特定的基因组位点。其中两种工具,锌指核酸酶(ZFNs)和转录激活因子样效应核酸酶(TALENs)。是成熟的基于蛋白质的系统,可在特定基因组位点引入双链断裂(DSB)。然后将编码目的转基因并通过同源臂连接到切割位点的供体 DNA 构建体共同引入可用于位点通过同源定向修复 (HDR) 进行定向整合。许多团队已经利用这种策略来整合不同的 RG。此外,随着安全基因组基因座的发现,研究人员有机会使用这些编辑工具进行安全转基因。例如,几个研究团队已经用 RG 改造了细胞在腺相关病毒整合位点 1 (AAVS1) 使用 ZFN 和 TALEN。这是一个安全港,转基因可以在不影响内源基因活性的情况下以可预测的方式整合和发挥作用。这一策略为消除任何潜在的有害影响打开了大门,但 ZFN 和 TALEN 的一个缺点是它们的设计和构造具有挑战性且昂贵,这限制了它们的广泛使用。
CRISPR* 和 CRISPR 相关蛋白 9 (Cas9) 于 2013 年成为首选的基因组编辑工具,因为它比 ZFN 和 TALEN 更容易设计且实施成本更低。 CRISPR/Cas9 系统利用 Cas9 核酸内切酶除了引导 RNA (gRNA) 之外,还可以在基因组的特定位点引入 DSB。这两个组件可以在单个质粒中编码,当与供体质粒配对时,还可以在感兴趣的位点进行基于 HDR 的转基因整合。重要的是,CRISPR/Cas9 也被证明比以前使用的编辑工具具有更高的效率。 它还具有简单的设计、高特异性和相对较高的效率,使其成为靶向整合 RG 的有前途的方法,进而对细胞进行惰性、安全和有效的分子遗传成像。这项研究的目的是开发一种新的 CRISPR/Cas9 系统,以在 AAVS1 安全港对细胞进行工程改造,以共同表达选择标记和双模式 RG,并利用分子-基因成像
方法和材料
AAVS1 靶向 CRISPR-Cas9 和供体质粒
pCas-Guide-AAVS1、pCas-Guide-Scramble 和 pAAVS1-puroDNR 构建体购自商业供应商 (OrigeneRockvilleMD)。pCas-Guide-AAVS1 质粒包含驱动 Cas9 核酸内切酶表达的巨细胞病毒启动子 (pCMV)基因和 U6 启动子驱动靶向 AAVS1 位点的 gRNA 表达。pCas-Guide-Scramble 质粒类似,但编码的 gRNA 不靶向任何特定的基因组位点。pAAVS1-puroDNR 质粒包含左侧和与 AAVS1 位点 CMV 增强剂和磷酸甘油酸激酶 1 启动子 (pPGK) 的右同源臂,驱动嘌呤霉素抗性基因的表达。先前在 Ronald 实验室构建的 LV pEF1a-tdT-P2A-Luc2 载体包含人延伸因子 la 启动子 ( pEF1α) 驱动荧光 RGtdTomato (tdT) 和产生萤火虫萤光素酶蛋白 (FLuc) 的密码子优化的生物发光 RG 萤火虫萤光素酶 (Luc2) 的表达。高效自切割猪 teschovirus-1 肽 (P2A)27. pEF1a-tdT-P2A-Luc2 盒通过 PCR 扩增并使用融合克隆 (Takara Bio, Mountain View, CA) 克隆到 pAAVS1-puroDNR 构建体中用 ApaI 和 FseI (New England Biolabs Inc, Ipswich MA) 消化 pAAVS1-puroDNR。这种新的供体载体被称为 pAAVS1-puro pEF1α-tdT-P2A-Luc2-DNR。
细胞和细胞工程
人胚胎肾 (HEK293T;ATCC Manassas VA) 细胞维持在 Dulbecco 改良 Eagle 培养基 (Thermo Fisher OntarioCA) 中,该培养基含有 10% 胎牛血清和 1% 青霉素/链霉素,37C 和 5% CO2。转染前一天,将细胞接种在六孔中板,密度为每孔 7x10 个细胞。按照制造商的建议,用 Lipofectamine 3000 转染细胞质粒或 pAAVS1-puro-pEF1a-tdT-P2A-Luc2-DNR 和 pCas-Guide 打乱质粒各 0.5 ug,与 1 uL P3000 试剂、50 uL Opti-MEM 培养基和 0.75 uL Lipofect amine 3000 混合。转染嘌呤霉素后 12 天将tibiotic(0.6ug / mL)添加到生长培养基中,并通过每天更换培养基来维持嘌呤霉素选择7天。由此产生的嘌呤霉素抗性细胞群称为我们的混合细胞群(MCP)。
AAVS1 整合分析
使用 DNeasy Blood and Tissue 试剂盒(QIAGEN Ontario, CA)从 MCP 中提取基因组 DNA(gDNA)。为了检测 AAVS1 位点的整合,制作引物以 PCR 扩增同源外 AAVS1 基因组位点之间的 5 和 3 连接。为5'连接设计的PCR引物为:5-AGGCAGGTCC TGCTTTCTCTGAC-3(正向引物与AAVS1位点互补)和5-TGCCTGCTCTTTACTGAA GGCTC-3(与嘌呤霉素抗性基因互补),潜在1.1 kb PCR 产物:对于 3iunction 是 5'-CCTGGAAGTTG CCACTCCAG-3(与供体盒中的 poly A 尾互补的正向引物)和 5-AAGGC AGCCTGGTAGACAGG-3'(与 AAVS1 位点互补的反向引物),潜在 1.4kb PCR 产物。在确认 AAVS1 引导 MCP 包含正确编辑的细胞后,将 MCP 连续稀释以在 96 孔板的每个孔中获得单个细胞。在细胞扩增后,我们从每个克隆群体中分离出 DNA使用与 MCP 相同的 PCR 引物再次评估 QuickExtract DNA 提取溶液(EpicentreMadisonWand AAVS1 整合。使用 Nucleospin 凝胶和PCR 净化试剂盒(Macherey NagelDuren Germany)和 PCR 产物在伦敦区域基因组学中心(Robarts Research Institute,London,ONCanada)进行测序。
报告基因功能
为了评估 tdTRG 功能,使用 EVOS FL aut 2 显微镜(Thermo Fisher Scientific)获得荧光图像。BLI 实验一式三份进行并用于评估 Luc2 RG 功能 BLI 信号和细胞数之间的关系,以及不同细胞传代中的 Luc2 RG 表达水平数字。为了评估 Luc2 RG 功能以及 BLI 信号和细胞编号之间的关系,将 HEK293T 细胞以每孔 1x1045x101x101.5x10 和 2.5x10 个细胞的浓度接种在 24 孔板中。为了评估增加细胞传代数对 Luc2 RG 表达的影响,将 5x10 细胞接种在 81012 和 14 代的 24 孔板中。对于所有板的 BLI,将 5 μL D-荧光素(0.1 mg/mL Perkin Elmer,Waltham MA)添加到每口井在使用混合光学/X 射线扫描仪(IVIS Lumina XRMS In Vivo Imaging System;PerkinElmer)收集图像前 5 分钟。使用 LivingImage 软件(PerkinElmer)分析 BLI 信号以确定平均辐射亮度(p/s/cm/ sr) 每口井。
动物研究
以下协议是按照加拿大动物护理委员会和西方大学动物护理委员会关于实验室动物护理和使用的指南进行的。本研究使用 6-8 周大的雌性 NUNUnude 小鼠 (NU-Foxn1n=5) ( Charles Rivers,Wilmington,MA)。每只小鼠在左后腹皮下注射 2.5x10Clone 10 HEK-293T 细胞。在第 037、14、21 天,在与上述相同的混合光学/X 射线扫描仪上进行 BLI,和28 只注射后的小鼠用 100% 氧气中的 2% 异氟醚麻醉,使用连接到活性炭过滤器上的鼻锥。麻醉小鼠腹膜内注射 150uL D 荧光素 (30mg/mL) 并捕获生物发光图像长达45 分钟。使用 LivingImage 软件 (PerkinElmer) 分析 BLI 信号,并通过在植入部位上绘制感兴趣区域来确定平均辐射 (p/sec/cm/sr)。 45 分钟成像期间的峰值平均辐射用于在每个成像时间点对每只小鼠进行量化。
组织学
在终点处,通过异氟醚过量处死小鼠,并从左后腹取出HEK293T生长组织。将组织固定在 4% 多聚甲醛中,然后在 30% 蔗糖的 PBS 中冷冻保存 24 小时。冷冻保存后,将组织浸入最佳切割温度并使用液氮冷冻。使用 Leica CM350 低温恒温器系统(Leica BiosystemsWetzlarGer)进行冷冻切片许多)以获得 14um 冷冻切片。冷冻切片用兔抗萤火虫荧光素酶一抗(ab21176Abcam,Cambridge,UK)和山羊抗兔 Alexa Fluor 488 二抗(ab150077 Abcam)染色,以评估 FLuc 的存在或仅用山羊抗兔 alexa fluor 488 二抗作为 FLuc 存在的对照,以及用于定位细胞核的 4,6-二脒基-2-苯基吲哚 (DAPI) 使用 ZeissLSM800 共聚焦显微镜(ZeissOberkochenGermany)对切片进行成像。
统计数据
使用 GraphPad PRISM 7 软件进行统计分析。为了比较接种的细胞数与体外 BLI 信号,我们进行了 Pearson 相关测试。为了评估体外 BLI 信号与传代次数的差异,我们进行了 Tukey 的多重比较测试。为了评估体内 BLI 信号随时间的差异,我们使用具有事后多重比较检验的弗里德曼检验。所有实验的 p 值为 0.05 被认为具有统计学意义。
研究内容
1.使用 CRISPR/Cas9 多模态报告基因 (RG) 系统在 AAVS1 位点改造细胞
pAAVS1-puro-pEF1a-tdT-P2A-Luc2-DNR质粒被开发用于与pCas Guide-AAVS1质粒结合使用,将多个成像RG(tdT和Luc2)整合到细胞的AAVS1安全基因组港中。pAAVS1-puro-pEF1a-tdTP2A-Luc2-DNR, pCas-guide-AAVS1, 和pCas-GuideScramble的质粒主要特点分别如图 1A-C 所示。为在细胞的 AAVS1 位点实现 RG 表达而进行的基因组编辑步骤如图 1D 所示。
为了确定 CRISPR/Cas9 系统是否可以有效地编辑具有大 RG 构建体(~6.3kb)的细胞的 AAVS1 位点,将 HEK293T 细胞与 pCas-Guide-AAVS1 和 pAAVS1-puro pEF1a-tdT-P2A-Luc2-DNR 质粒共转染或 pCas-Guide Scramble 和 pAAVS1-pur-pEF1a-tdT-P2A-Luc2-DNR 质粒。正如预期的那样,两种转染都产生了嘌呤霉素抗性细胞群,但我们使用 5' 基因组 - 供体盒连接处的引物进行的 PCR AAVS1 整合测试(图 2A)揭示了仅在与 AAVS1 靶向 gRNA 共转染的 MCP 中的条带(图 2B). 然后建立和扩了 26 个克隆细胞群,并使用 PCR 分析测试在 AAVS1 位点的整合。在测试的 26 个克隆中,只有第 10 个克隆群(HEK293T 克隆 10)显示供体盒整合到AAVS1 位点使用引物组用于 3 和 5 基因组供体盒连接。因此正确编辑的嘌呤霉素抗性细胞百分比为 3.8%。PCR 产物的凝胶提取和测序揭示了预期的 DNA 序列,进一步验证了 AAVS1 编辑在这个细胞群中使用我们的供体盒(图 2D,E)。
在克隆群体中的 AAVS1 位点编辑确认后,进行体外实验以确定整合的 RGs 是否在这些细胞中起作用。 HEK293T 克隆 10 细胞的明场和荧光图像显示功能性 tdTex - 表达(图 3A)。每孔不同数量的细胞(1x10、5x10、1x101.5x10 和 2.5x105)也用 BLI 成像以可视化 Luc2 表达(图 3)。 3B),细胞数与BLI信号呈显着正相关(p<0.05:R2=0.9988;图3C)。随着传代数增加的细胞BLI(PP10P12P14)BLI信号无显着差异(p >0.05,图 3D)。
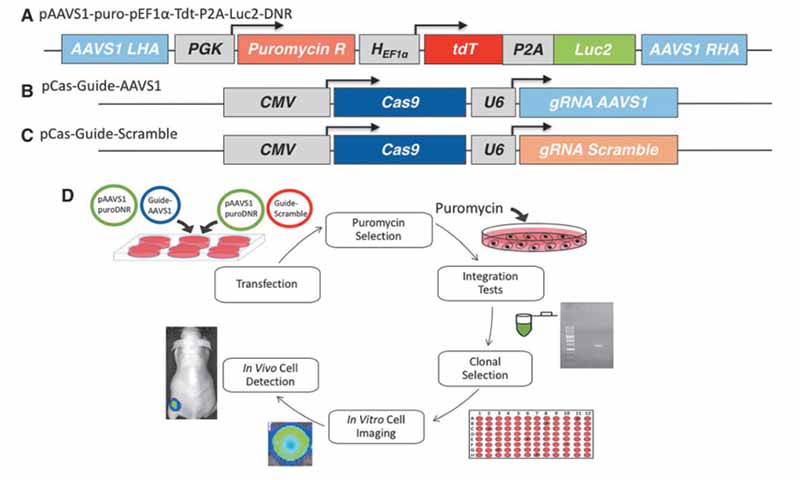
图1. 腺相关病毒整合位点 1 (AAVS1) 靶向 CRISPR-Cas9 双质粒系统和基因组编辑方案。 (A) pAAVS1-puro-pEF1a-tdT-P2A-Luc2-DNR (B) pCas-Guide-AAVS1 质粒和 (C) pCas-Guide-Scramble 质粒的矢量图。 (D) 用 CRISPR-Cas9 质粒转染细胞,并在转染后 12 天将嘌呤霉素抗生素添加到转染群体中以进行细胞选择。 产生的混合细胞群 (MCP) 用结 PCR 进行评估,以验证供体盒整合到一些细胞中的 AAVS1 位点。 培养单克隆种群并评估成功的基因组编辑。 成功编辑的克隆在体外成像以确定报告基因功能,并在体内成像以监测细胞随时间的活力
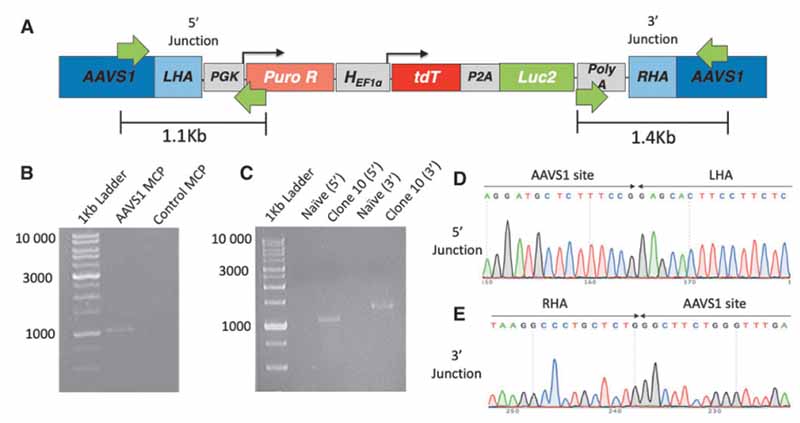
图2. 在 AAVS1 位点编辑的人胚肾 (HEK293T) 细胞的连接 PCR 分析。 (A) 同源定向修复介导的供体盒插入后 AAVS1 位点的图示,绿色箭头代表 PCR 引物及其各自的产物大小,如下所示。 (B) 混合细胞群 (MCP) 的 PCR 评估显示 pCas-Guide-AAVS1 和 pAAVS1-puroDNRtdT-Fluc 质粒转染群存在正确大小的单条带。控制 MCP 中不存在条带。 (C) 单个克隆群体的 PCR 评估显示第十个克隆群体(克隆 10)对于 5¢ 连接和 3¢ 连接 PCR 测试具有正确的条带大小。没有注意到幼稚 HEK293T 细胞的条带。克隆 10 个 PCR 产物的测序显示 AAVS1 位点和左同源臂 (LHA) (D) 之间的 5¢ 连接点和右同源臂 (RHA) 和 AAVS1 位点 (E) 之间的 3¢ 连接点, 进一步证实AAVS1 位点克隆 10 细胞群中的基因组编辑
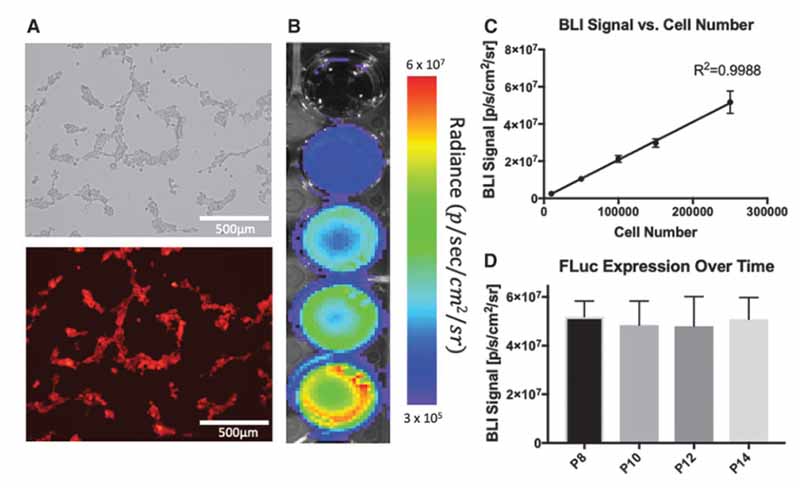
图3. 报告基因功能的体外研究。 (A) 明场图像和荧光显微镜图像显示 HEK293T 克隆 10 细胞中的 tdTomato 表达。 (B) 增加 HEK293T 克隆 10 细胞数量的生物发光成像 (BLI) 显示萤火虫荧光素酶 (FLuc) 表达。 (C) 发现细胞数和 BLI 信号之间存在显着的线性相关性。 p < 0.05; R2 = 0.9988。 (D) HEK293T 克隆 10 细胞在体外多次传代中 FLuc 表达没有显着变化。 p > 0.05。
2. AAVS1 编辑细胞的纵向体内 RG 成像
接下来,我们进行了体内 BLI,以评估 AAVS1 编辑的细胞的生存能力超时。将 HEK293Tclone10 细胞 (2.5x10°) 注射到裸鼠的左后腹,并在注射后第0,3,7,14,21,和28 天进行 BLI。到第 7 天,在五只小鼠中的一只中观察到 BLI 信号的完全丧失(代表活细胞的丧失),因此该小鼠被排除在其余的成像时间点之外。在其余四只小鼠的所有时间点获得的每个 BLI 图像中都可以检测到信号。图 4A 显示了随着时间的推移为一只小鼠采集的代表性图像。从第 0 天到第 7 天观察到 BLI 信号下降,这可能是由于细胞死亡,随后随着细胞在后侧形成团块而 BLI 信号增加。这种趋势在所有四只小鼠的信号丢失和复发是一致的,所有四只小鼠的平均 BLI 信号从第 7 天到第 28 天显着增加(p<0.05;图 4B)。
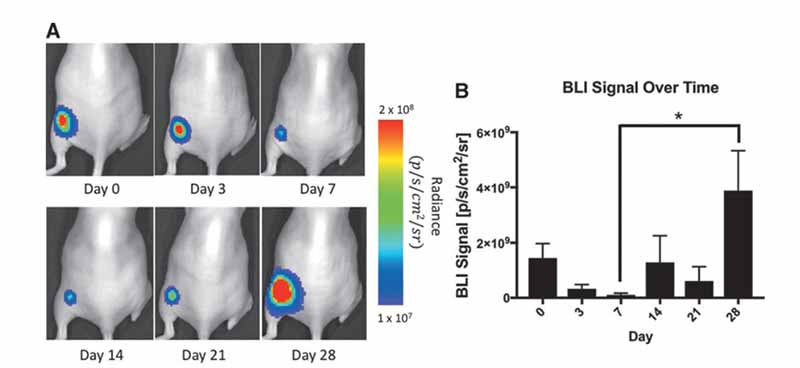
图4. 随着时间的推移,AAVS1 编辑的细胞的体内 BLI。 (A) 将表达 FLuc 的 AAVS1 编辑的 HEK293T 细胞(克隆 10)的 BLI 植入代表性小鼠的左后腹,在植入后第 0、3、7、14、21 和 28 天成像。 在前 7 天观察到 BLI 信号的初始下降,随后 BLI 信号增加。 (B) 随着时间的推移,每幅图像中平均辐射的量化显示,从第 7 天到第 28 天,BLI 信号显着增加(p < 0.05;n = 4 只小鼠)。
3. 组织学
为了确认 HEK293T 克隆 10 生长组织具有 Luc2 RG 表达,对冰冻切片进行染色以确认萤火虫荧光素酶蛋白 (FLuc) 的存在。荧光图像显示染色的 HEK293T 克隆 10 生长组织中的 FLuc(图 5A)与对照 HEK293T 克隆 10 生长相比组织(图 5B)。
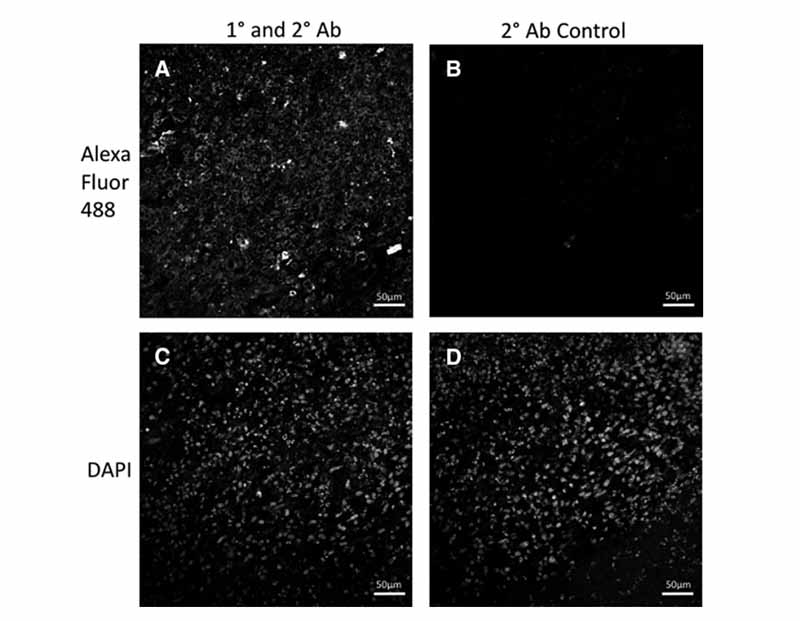
图5. HEK293T 生长组织的代表性图像显示 FLuc 染色阳性 (A),仅在二次染色的切片中不存在 (B)。 底行 (C, D) 显示相同部分的 DAPI 染色
结论与讨论
基于报告基因的体内细胞追踪是癌症进展和癌症治疗等疾病的临床前研究以及基于细胞的疗法的功效的一种有价值的工具,因为它可以提供有关位置、分布和生存能力的信息。
然而,这种方法被潜在的生物学和在考虑翻译时由于在随机基因组位点稳定整合 RGs 引起的安全问题所混淆。 例如,之前的研究表明,与临床前研究中的非工程细胞相比,病毒介导的工程细胞可以改变行为。这也产生了深远的临床后果,如四名患有 x 连锁严重联合免疫缺陷病的患者在注射逆转录病毒工程 CD34+ 细胞后患上白血病并死亡33。 潜在的行为改变和传统细胞工程技术的整体安全性的不确定性表明,需要一种更安全、更有效的方法来对细胞群进行基因标记,以跟踪、治疗或靶向疾病。 我们探索了使用 CRISPR/Cas9 技术对 AAVS1 安全基因组位点的细胞进行基因改造,以实现细胞活力随时间推移的体内 RG 成像。 作为原理证明,我们证明了我们的双质粒 AAVS1 靶向 CRISPR/Cas9 系统可用于在具有多个 RG(即 tdT 和 Luc2)的 AAVS1 基因座处对细胞进行基因编辑,编码的 RG 具有功能性和稳定性,并且 可以使用非侵入性 BLI 在小鼠中随时间监测工程细胞的活力。
CRISPR/Cas9 于 2013首次被报道为基因组编辑工具,此后被广泛用作转基因敲入研究的相对简单且有效的技术,此外,非成像研究已使用 CRISPR/Cas9 系统在 AAVS1 基因座处整合各种转基因。尽管其他基因组编辑技术已经存在了一段时间(例如 ZFNs 和 TALENs,但 CRISPR 的改进效率经常被讨论与这些工具相关,据报道,“敲入”效率从 0.14% 到 66%,具体取决于人类细胞类型以及用于引入 Cas9 基因/mRNA/蛋白质 gRNA 和供体盒的方法。敲入的一个考虑因素是较大的插入盒会导致编辑效率下降。出于我们的目的,这对在质粒构建过程中可以使用的 RG 数量和大小,然而,由于 CRISPR/Cas9 系统已被证明能够将大型 RG 构建体插入特定基因组位点,我们设计了我们的供体质粒来编码两个成像 RG,这些 RG 通过使用 2A 肽以及抗生素选择标记由单个启动子驱动。在这项工作中,3.8% 的嘌呤霉素抗性 HEK-293T 细胞被正确编辑。与之前使用 CRISPR Cas9 编辑 AAVS1 位点的基因组编辑研究相比,这是相对较低的效率。但是对于我们构建的大小,这是可以预料的.据我们所知,我们是第一个报告大型双 RG 表达盒(~6.3kb)可以在 AAVSI 站点与 CRISPR/Cas9 技术集成的报告。在目前的研究中,tdT RG 允许我们进行荧光显微镜检查,但未来我们可能会通过去除嘌呤霉素抗性基因并使用 tdT 表达来进行荧光激活细胞分选和扩大工程细胞群来限制我们构建体的大小。更高代数的细胞已被证明过去已经改变了基因表达。我们的实验依赖于随着时间推移稳定的 RG 表达,以准确检测细胞并比较细胞增殖随着时间的推移。因此,我们测试了随着传代次数增加的细胞群中 RG 表达的变化,但没有发现任何显着差异。重要的是,RGs 使我们能够使用基于 FLuc 的 BLI,使我们能够在细胞注射后直接可视化工程细胞群并评估 由于 FLuc 需要 ATP 作为光产生的辅助因子,因此随着时间的推移细胞的活力。BLI 还能够在一只小鼠的早期时间点快速且相对便宜地筛查异种移植排斥,从而使我们能够将这种动物排除在研究的其余部分之外。该系统目前仅限于临床前研究,可以很容易地对其进行修改,以表达临床成像模式(如磁共振成像正电子发射断层扫描 (PET) 或光声断层扫描)感兴趣的替代 RG。
我们的 CRISPR/Cas9 方法并非没有限制,需要在未来的研究中解决。首先,与慢病毒系统相比,CRISPR/Cas9 质粒系统的整合效率要低得多。我们使用相对较大的供体构建体(10.6 kb 总质粒大小和 6.3 kb 预期插入)很可能降低了我们系统的效率,因为更大的插入更难敲入以及低于理想的转染效率。未来的工作应该着眼于减少供体盒的大小和整体质粒大小(例如, 通过限制 RGs 的数量)来提高转染效率和随后的编辑效率 在对阳离子转染剂特别是原代细胞具有抗性的细胞中,使用物理基因转移方法(例如微孔/核转染/磁转染)也可以提高转染效率。或者,也可以探索使用附加型病毒载体。例如腺相关病毒或非整合慢病毒载体,以将所有必要的成分递送到细胞中。还有研究表明,用 Cas9-gRNA 核糖核蛋白复合物转染细胞可以提高切割效率,从而提高敲入效率。 56-58另一个考虑因素是基因组无论是通过 CRISPR Cas9 脱靶切割还是正常的质粒整合,编辑方法都不能完全消除随机整合事件。Fu 等人表明,精心设计的 agRNA 可以减少脱靶效应,而 CRISPR 酶上的新 Cas9 类似物已减少脱靶效应正在开发中。6061 此外,Chen 等人也证明了这一点。抗生素选择有助于更多数量的脱靶效应。通过实施荧光激活细胞分选,如 Raul Bressen 等人所示。嘌呤霉素选择可以从协议中删除,从而实现更有效的选择过程和更少的随机整合事件。我们方法的另一个限制是必须将集成在 AAVS1 站点的细胞与那些包含随机集成盒的细胞分开。测试使用 CRISPR/Cas9 系统所需的单个克隆群体的过程更加费力,并且可以减少原始细胞群体的自然细胞异质性。尽管此处未进行,但可以将多个克隆细胞群汇集在一起,以减轻细胞异质性的损失,但仅选择那些已正确编辑的细胞的新方法将是非常有价值的。通过实施其中一些或许多方法,我们计划继续改进我们的 CRISPR/Cas9 递送系统。我们认为,通过这些改进,该系统将成为广泛适用和高度有用的技术,用于广泛的癌症和基于细胞的治疗分子遗传成像在临床前和潜在的临床研究中。
结论
这项工作描述了双质粒系统的开发,以通过分子成像 RGs 对细胞进行 AAVS1 靶向 CRISPR/Cas9 基因组编辑。我们能够首次证明 CRISPR/Cas9 系统可用于执行大型整合 构建编码抗生素选择标记和多个 RGs 到 AAVS1 安全港,以实现基于体内 RG 的纵向细胞追踪 可以很容易地在培养中扩增(例如,T细胞)。通过这些改进,这种基因组编辑系统将在未来基于 RG 的体内细胞追踪研究中广泛使用。
大家都在看
-
THP-1细胞培养指南及常见问题:THP-1细胞培养基:90% 1640+10% FBS+PS+ 0.05 mM 2-巯基乙醇(2-mercaptoethanol),如果THP-1细胞密度达80%-90%,即可进行传代培养,传代比例:1:2至1:3,THP-1细胞有密度依赖性,低密度时细胞···...
阅读详情 -
vero细胞培养条件及方法:vero细胞培养基MEM+10%FBS+1%PS,如果vero细胞密度达80%-90%,即可进行传代培养,传代比例:1:2至1:3,每周 2-3次,vero细胞生长条件:气相:95%空气+5%二氧化碳;温度:37℃...
阅读详情 -
MCF-7细胞培养条件及注意事项:MCF-7细胞培养基89%DMEM+10%FBS+1%PS+0.01mg/ml insulin,培养条件气相:95%空气+5%二氧化碳;温度:37℃,培养箱湿度70%-80%,MCF-7细胞贴壁较慢,处理后最好48h后再观察,MCF-7细胞培养需要加···...
阅读详情 -
RAW 264.7细胞培养传代及冻存处理:需要准备培养基:DMEM+10%FBS+PS、培养皿、无血清冻存液,RAW 264.7细胞传代步骤如下,a、将含有1mLRAW 264.7细胞悬液的冻存管在 37℃水浴中迅速摇晃解冻,加4 mL培养基混合均匀;b、在1···...
阅读详情 -
MDCK细胞培养方法及应用:MDCK细胞培养基:MEM(ATCC改良)+10%FBS+PS,生长条件;气相:95%空气+5%二氧化碳;温度:37℃,MDCK细胞被广泛用作远曲小管或集合管的模型,还可用于代谢研究和Pg级药物与药物相互作用研究以及观察流···...
阅读详情 -
乳腺癌研究常用细胞系及其优化实验方案:绝大多数乳腺癌都是起始于乳腺导管细胞,只有10%的乳腺癌起始于乳腺小叶细胞,另有一些罕见起源的乳腺癌种类,由于乳腺附近存在淋巴结和淋巴腺,这也是乳腺癌易于扩散转移的原因之···...
阅读详情
相关问答
-
细胞名称:A7r5细胞系(A7R5大鼠胸大动脉平滑肌细胞)客户问题:细胞中黑色的是什么?原因分析:1.棉球纤维、凋亡细胞片、血清蛋白,或一些无血清培养基添加因子后的因子析出物,属于正常现象;2.如果是传代后细胞堆···...
阅读详情 -
细胞增殖速度怎么变得这么慢了?细胞发生病变,出现细胞变圆、从培养瓶壁脱落又是什么情况?要疯了,培养细胞怎么就这么难呢~实验过程中存在的“幽灵”,即使是经验丰富的老研究员也不得不面对,没错,它就是支原体感···...
阅读详情 -
胎牛血清和小牛血清的差别在哪里? 胎牛血清和小牛血清的差别在哪里? 胎牛血清(FBS) :从八月龄胎牛心脏穿刺取血。适用于专业的研究和试验,包括干细胞研究、免疫分析和抗体生产。 新生牛血青/小牛血清(NBCS) :从自出···...
阅读详情 -
适合细胞长期保存的温度是多少? 适合细胞长期保存的温度是多少? 细胞长期保存温度是-130°C或更低。液氮罐中气态层温度在-140°C至-180°C之间细胞可保存在气态层或浸入液氮中,如果可以最好保存在气态层,因为这样···...
阅读详情 -
如何在细胞铺板时避免“边缘效应”? 如何在细胞铺板时避免“边缘效应”? 以下这三点一定要注意!细胞实验铺板时,为避免“边缘效应”,以应用96孔板的中间60孔为最佳,一般四周的一圈边缘孔不养细胞,只做空白或阴性···...
阅读详情 -
如何收获需要冻存的细胞?最佳是什么时候?如何收获需要冻存的细胞?最佳是什么时候?用来冻存的细胞一般选择在细胞约铺满90%的时候,这时细胞生长状态好,细胞数量也多并且在收获细胞前24小时换一次培养液。收获用来冻···...
阅读详情